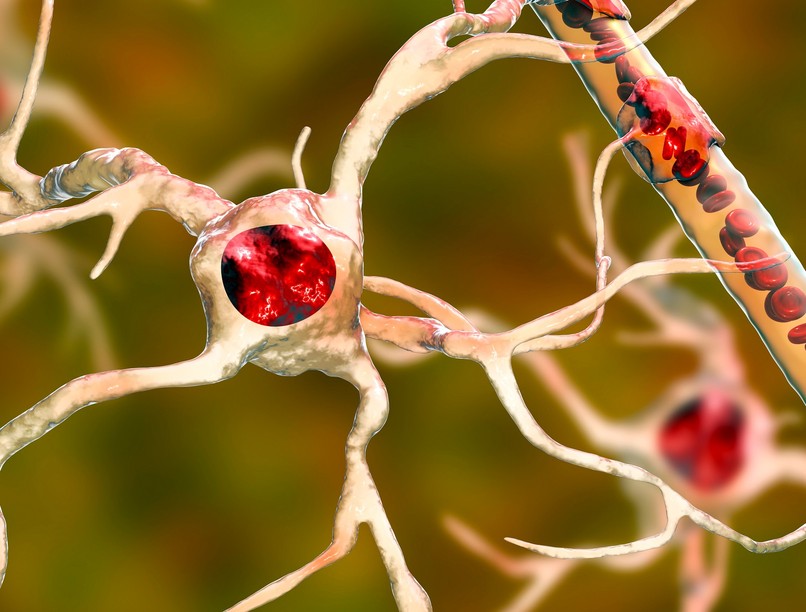
A módszer, amely a glioblasztóma agydaganatot körülvevő asztrocitákat veszi célba, kiirtotta a tumorsejteket és meghosszabbítta az élettartamot állatmodellekben.
A Tel Avivi Egyetemen végzett úttörő tanulmány eredményesen felszámolta a glioblasztómát, az agyrák rendkívül halálos típusát, melynél a betegek átlagosan 15 hónapos várható élettartammal néznek szembe.
A glioblastoma multiforme (GBM) a leggyakoribb és rosszindulatú glióma felnőtteknél. A GBM-vel diagnosztizált betegek szomorú prognózissal néznek szembe, átlagosan 15 hónapos várható élettartammal.
Mi az a GBM?
A glioblastoma multiforme az egyik legagresszívabb formája az agydaganatnak. A daganatok előrehaladtával a betegek valószínűleg súlyos szövődményeket tapasztalnak, mint például epilepsziás rohamok, peritumorális ödéma és intracranialis hypertonia. A GBM rendkívüli agresszivitása számos kóros jellemző eredménye. Például a GBM diffúz módon terjed a központi idegrendszerben, lehetővé téve számára, hogy elkerülje a sebészeti beavatkozásokat.
Amikor a GBM átnyomja magát a parenchymán, súlyos szövetkárosodást okoz, és megzavarja a központi idegrendszer működését. Ezenkívül a GBM hatékonyan ellenáll a hagyományos sugárzásnak és kemoterápiáknak.
Agydaganat: három tünet, ami gyanakvásra ad okot - olvasson tovább >>
Új módszer a GBM agydaganat ellen
A módszer, amely a glioblasztóma agydaganatot körülvevő asztrocitákat veszi célba, kiirtja a tumorsejteket és meghosszabbítja az élettartamot állatmodellekben.
A kutatók egy olyan módszerrel érték el az eredményt, amelyet két olyan kritikus agyi mechanizmus felfedezése alapján fejlesztettek ki, amelyek támogatják a daganat növekedését és túlélését:
- az egyik megvédi a rákos sejteket az immunrendszertől,
- míg a másik biztosítja a daganatok gyors növekedéséhez szükséges energiát.
A munka során megállapították, hogy mindkét mechanizmust az asztrocitáknak nevezett agysejtek irányítják, s ezek hiányában a tumorsejtek elpusztulnak és megsemmisülnek.
A tanulmányt Rita Perelroizen doktorandusz vezette, Dr. Lior Mayo, a Shmunis School of Biomedicine and Cancer Research és a Sagol School of Neuroscience munkatársainak felügyelete alatt, az amerikai National Institutes of Health (NIH) professzorával, Eytan Ruppinnal együttműködve.
A tanulmány a Brain című folyóiratban jelent meg, és külön kommentárral emelték ki.
A kutatók kifejtették:
"A glioblasztóma egy rendkívül agresszív és invazív agydaganat, amelyre nincs ismert hatékony kezelés. A tumorsejtek rendkívül ellenállóak minden ismert terápiával szemben, és sajnos a betegek várható élettartama az elmúlt 50 évben nem nőtt jelentősen. Eredményeink ígéretes alapot biztosítanak a glioblasztóma és más típusú agydaganatok kezelésére szolgáló hatékony gyógyszerek kifejlesztéséhez."
Dr. Mayo: új szemszögből közelítettük meg a glioblasztóma kihívását!
"Ahelyett, hogy a daganatra koncentráltunk volna, a támogató mikrokörnyezetre, vagyis a tumorsejteket körülvevő szövetre összpontosítottunk. Konkrétan az asztrocitákat vizsgáltuk - a normális agyműködést támogató agysejtek fő osztályát, amelyet körülbelül 200 évvel ezelőtt fedeztek fel, és csillagszerű alakjukról neveztek el."
"Az elmúlt évtizedben az általunk és mások által végzett kutatások további asztrocita funkciókat tártak fel, amelyek vagy enyhítik, vagy súlyosbítják a különböző agyi betegségeket. A mikroszkóppal végzett vizsgálatok alatt észrevettük, hogy aktivált asztrociták veszik körül a glioblasztóma tumorokat. E megfigyelés alapján nekiláttunk, hogy megvizsgáljuk az asztrociták szerepét a glioblasztóma tumorok növekedésében".
A kutatók egy olyan állatmodell segítségével, amelyben ki tudták iktatni a tumor körüli aktív asztrocitákat, megállapították, hogy az asztrociták jelenlétében a daganat 4-5 héten belül megölte az összes glioblasztóma-tumorral rendelkező állatot.
Egyedülálló módszert alkalmazva a daganat közelében lévő asztrociták specifikus kiirtására, drámai eredményt figyeltek meg: a rák napokon belül eltűnt, a kezelést minden állat túlélte, sőt, a legtöbb állat a kezelés abbahagyása után is életben volt.
Dr. Mayo: a mögöttes mechanizmusok érdekeltek
"Asztrociták hiányában a tumor gyorsan eltűnt, és a legtöbb esetben nem volt visszaesés, ami azt jelzi, hogy az asztrociták nélkülözhetetlenek a tumor progressziójához és túléléséhez. Ezért megvizsgáltuk a mögöttes mechanizmusokat: Hogyan alakulnak át az asztrociták a normális agyi tevékenységet támogató sejtekből a rosszindulatú daganat növekedését támogató sejtekké?"
E kérdések megválaszolása érdekében a kutatók összehasonlították az egészséges agyból és a glioblasztóma tumorokból izolált asztrociták génexpresszióját.
Két fő különbséget találtak - ezáltal azonosították azokat a változásokat, amelyeken az asztrociták átesnek, amikor glioblasztómának vannak kitéve.
Az első változás a glioblasztómára adott immunválaszban történt
"A tumor tömege akár 40%-ban tartalmaz immunsejteket - főként a vérből vagy magából az agyból toborzott makrofágokat. Továbbá az asztrociták képesek olyan jeleket küldeni, amelyek immunsejteket hívnak az agy olyan helyeihez, amelyek védelemre szorulnak. Ebben a tanulmányban azt találtuk, hogy az asztrociták továbbra is betöltik ezt a szerepet glioblasztóma tumorok jelenlétében. Amint azonban a megidézett immunsejtek elérik a tumort, az asztrociták "rábeszélik" őket, hogy "váltsanak oldalt" és támadás helyett támogassák a tumort."
"Konkrétan azt találtuk, hogy az asztrociták megváltoztatják a toborzott immunsejtek azon képességét, hogy közvetlenül és közvetve is megtámadják a daganatot - ezáltal védik a daganatot és elősegítik annak növekedését" - mondja Dr. Mayo.
Megvonták a számára éltető táplálékot a agytumortól
A második változás, amellyel az asztrociták támogatják a glioblasztómát, azáltal történik, hogy módosítják az energiához, "éltető táplálékhoz" való hozzáférésüket - a koleszterin termelésén és a tumorsejtekbe történő átvitelén keresztül.
A tudósok évek óta feltételezik, hogy a legtöbb glioblasztóma koleszterinfüggő, s hogy ez új gyógyszerek kifejlesztésére ad lehetőséget. A glioblasztómák 90 százaléka rendelkezik a "hiperaktív jelzőúttal" a koleszterinre. Ez azt jelenti, hogy a sejtjeik programozása miatt magukba "szippantják" az LDL-koleszterint, mely miatt tovább növekednek.
Dr. Mayo:
"A rosszindulatú glioblasztóma sejtjei gyorsan osztódnak, ami nagy mennyiségű energiát igényel. Mivel a vérben lévő energiaforrásokhoz való hozzáférést a vér-agy gát akadályozza, ezt az energiát magából az agyban termelt koleszterinből - nevezetesen az asztrociták "koleszteringyárában", amely általában az idegsejteket és más agysejteket látja el energiával - kell beszerezniük.
"Felfedeztük, hogy a daganatot körülvevő asztrociták fokozzák a koleszterintermelést, és ellátják vele a rákos sejteket. Ezért azt feltételeztük, hogy mivel a daganat fő energiaforrásként ettől a koleszterintől függ, ennek az ellátásnak a megszüntetése kiéhezteti a daganatot"."
Ezután a kutatók úgy alakították át a tumor közelében lévő asztrocitákat, hogy azok ne expresszáljanak többé egy speciális, koleszterint szállító fehérjét (ABCA1), és így megakadályozták, hogy koleszterint szabadítsanak fel a tumorba.
Az eredmények ismét drámaiak voltak:
mivel a tumor nem jutott hozzá az asztrociták által termelt koleszterinhez, lényegében néhány nap alatt "éhen halt".
Ezek a figyelemre méltó eredmények mind állatmodelleken, mind emberi betegekből vett glioblasztóma-mintákon születtek, és összhangban álltak a kutatók koleszterin kiéheztetésen alapuló hipotézisével.
Dr. Mayo megjegyzi:
"Ez a munka új megvilágításba helyezi a vér-agy gát szerepét az agyi betegségek kezelésében. Ennek a gátnak a normális célja az agy védelme azáltal, hogy megakadályozza az anyagok átjutását a vérből az agyba. Agybetegség esetén azonban ez a gát megnehezíti a gyógyszerek agyba juttatását, és a kezelés akadályának tekinthető."
"Eredményeink arra utalnak, hogy - legalábbis a glioblasztóma konkrét esetében - a vér-agy gát előnyös lehet a jövőbeli kezelések szempontjából, mivel egyedülálló sebezhetőséget teremt - a daganat függőségét az agyban termelt koleszterintől. Úgy gondoljuk, hogy ez a gyengeség egyedülálló terápiás lehetőséggé válhat."
A projekt során több száz humán glioblasztómás beteg adatbázisát is megvizsgálták, és a fent leírt eredményekkel korrelálták azokat.
"Minden egyes beteg esetében megvizsgáltuk azoknak a géneknek az expressziós szintjét, amelyek vagy semlegesítik az immunválaszt, vagy koleszterin alapú energiaellátást biztosítanak a tumornak. Azt találtuk, hogy azok a betegek, akiknél ezen azonosított gének expressziója alacsony volt, tovább éltek, ami alátámasztja azt az elképzelést, hogy az azonosított gének és folyamatok fontosak a glioblasztómás betegek túlélése szempontjából" - fejtették ki a kutatók.
Dr. Mayo zárógondolata
"Jelenleg a daganatot körülvevő asztrociták eltávolítására szolgáló eszközök állatkísérletes modellekben rendelkezésre állnak, de emberben nem. A kihívás most az, hogy olyan gyógyszereket fejlesszünk ki, amelyek a daganat növekedését elősegítő, az asztrocitákban zajló specifikus folyamatokat célozzák meg. Alternatív megoldásként a meglévő gyógyszereket át lehet alakítani, hogy gátolják az ebben a tanulmányban azonosított mechanizmusokat. Úgy gondoljuk, hogy a tanulmány által biztosított koncepcionális áttörések felgyorsítják a sikert a glioblasztóma elleni küzdelemben. Reméljük, hogy eredményeink alapul szolgálnak majd e halálos agydaganat és más agydaganattípusok hatékony kezelésének kifejlesztéséhez."
Olvasta már?
- Agydaganat kezelése: fontos eredményekre jutottak a kutatók
- Agydaganat kezelése gyógyszerrel: debreceni kutatók is kísérleteznek
- Hasogató fejfájás - ezekben az esetekben azonnal hívjon orvost
Mikortól magas a koleszterin? Ekkor van szükség gyógyszerre a szakorvos szerint
Kövesse az Egészségkalauz cikkeit a Google Hírek-ben, a Facebook-on, az Instagramon vagy a X-en,Tiktok-on is!