IDELVION 1000 NE por és oldószer oldatos injekcióhoz
Betegtájékoztató
1. Milyen típusú gyógyszer az IDELVION, és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer az IDELVION?
Az IDELVION egy hemofília elleni gyógyszer, amely helyettesíti a természetes IX-es véralvadási (koagulációs) faktort. Az IDELVION hatóanyaga az albutrepenonakog-alfa (rekombináns fúziós fehérje, albuminnal kapcsolt IX-es véralvadási faktor (rIX-FP)).
A IX-es faktor részt vesz a véralvadásban. A hemofília B-ben szenvedő betegeknél hiányzik ez a faktor, ami azt jelenti, hogy az ő vérük nem alvad meg olyan gyorsan, ahogy kellene, megnő a vérzési hajlam. A hemofília B-ben szenvedő betegeknél az IDELVION pótolja a IX-es faktort, ezzel lehetővé teszi náluk a véralvadást.
Milyen betegségek esetén alkalmazható az IDELVION?
Az IDELVION-t a szükséges IX-es faktor hiánya által okozott vérzés megelőzésére vagy kezelésére alkalmazható minden korcsoportban, a hemofília B-ben szenvedő betegeknél (más néven öröklött IX-es faktor hiány vagy Christmas betegség).
2. Tudnivalók az IDELVION alkalmazása előtt
Ne alkalmazza az IDELVION-t
- ha allergiás a hatóanyagra (albutrepenonakog-alfa) vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
- ha allergiás hörcsögfehérjére.
Figyelmeztetések és óvintézkedések
Nagyon ajánlott, hogy minden alkalommal, amikor IDELVIONT használ, rögzítse gondozási naplójában az alkalmazott termék nevét és gyártási számát, hogy nyomon követhető legyen az Ön által alkalmazott termék és a termék gyártási tételei.
Az IDELVION alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel.
- Allergiás (túlérzékenységi) reakciók előfordulhatnak. A készítmény nyomokban hörcsög fehérjét tartalmaz (lásd "Ne alkalmazza az IDELVION-t"). Ha a túlérzékenység (allergiás reakciók) tünetei jelentkeznek, Önnek azonnal abba kell hagynia a gyógyszer alkalmazását, és fel kell vennie a kapcsolatot a kezelőorvosával vagy az Ön kezelését felügyelő kezelő centrummal. A kezelőorvosának tájékoztatnia kell Önt a túlérzékenységi reakciók korai tüneteiről. Ezek közé tartozik a csalánkiütés, testszerte jelentkező bőrkiütés, mellkasi szorító érzés, sípoló légzés, alacsony vérnyomás (hipotonia) és az anafilaxia (súlyos allergiás reakció, ami súlyos légzési nehézséget vagy szédülést okoz)
- A IX-es faktorhoz köthető allergiás reakciók kockázata miatt az IDELVION első alkalmazását orvosi megfigyelés mellett kell végezni, ahol az allergiás reakciók megfelelő ellátása biztosítható.
- Az inhibitorok (semlegesítő ellenanyagok) képződése ismert szövődmény, melyet IDELVION-nal történő kezelés alatt jelentettek. Az inhibitorok megakadályozzák, hogy a kezelés hatása megfelelő legyen. Ha az IDELVION nem csillapítja az Ön vérzését, azonnal értesítse a kezelőorvosát. Önnél rendszeresen ellenőrizni kell az inhibitorok kialakulását.
- Ha Ön máj- vagy szívbetegségben szenved, vagy nemrégiben nagyobb műtéten esett át, tájékoztassa kezelőorvosát, mivel ilyenkor nagyobb a véralvadási (koagulációs) szövődmények kockázata.
- Amennyiben Önnél egy centrális vénás kanülre van szükség (az IDELVION beadásához), akkor a kezelőorvosának mérlegelnie kell a szövődmények, köztük a helyi fertőzések, baktériumok véráramba kerülésének (bakterémia), valamint a kanül bevezetésének helyén az érben kialakuló vérrög (trombózis) kockázatát.
Egyéb gyógyszerek és az IDELVION
- Feltétlenül tájékoztassa kezelőorvosát a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről.
Terhesség, szoptatás és termékenység
- Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
- Terhesség vagy szoptatás alatt az IDELVION csak egyértelmű javallat esetén alkalmazható.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Az IDELVION nem befolyásolja a gépjárművezetéshez és a gépek kezeléséhez szükséges képességeket.
Az IDELVION nátriumot tartalmaz
Ez a gyógyszer maximum 8,6 mg nátriumot (a konyhasó fő komponense) tartalmaz injekciós üvegenként, ami megfelel a nátrium ajánlott maximális napi bevitel 0,4%-ának felnőtteknél.
3. Hogyan kell alkalmazni az IDELVION-t?
Az Ön kezelésének elkezdését és annak ellenőrzését a véralvadási zavarok kezelésében jártas orvosnak kell végeznie. A gyógyszert mindig a kezelőorvosa által elmondottaknak megfelelően alkalmazza.
Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát.
Kezelőorvosa számolja ki az Önnek szükséges IDELVION adagot. Az Önnek szükséges IDELVION mennyiségét és az alkalmazás időtartamát az alábbi tényezők befolyásolják:
- a betegségének súlyossága,
- a vérzés helye és intenzitása,
- az Ön klinikai állapota,
- az Ön testtömege.
Az IDELVION-t vénába adott injekcióként (intravénásan, IV.) alkalmazzák, miután az ön kezelőorvosa vagy ápolója feloldotta a port a mellékelt oldószerrel. Ön vagy valaki más is beadhatja az IDELVION-t IV. injekcióként, de csak megfelelő képzés után.
Ha az előírtnál több IDELVION-t alkalmazott
Haladéktalanul vegye fel a kapcsolatota kezelőorvosával, ha több IDELVIONT alkalmazott, mint amennyit a kezelőorvosa javasolt.
Ha idő előtt abbahagyja az IDELVION alkalmazását
Ne hagyja abba az IDELVION alkalmazását a kezelőorvosa megkérdezése nélkül.
Feloldás és alkalmazás
Általános tudnivalók
- A port el kell keverni az oldószerrel (folyadék), fel kell szívni az injekciós üvegből, miközben a gyógyszert sterilen (csíramentesen) kell tartani. Az Ön kezelőorvosa megmutatja, hogyan kell elkészíteni az oldatot és hogyan kell helyesen felszívni az injekciós üvegből.
- Az IDELVION nem keverhető más gyógyszerrel vagy oldószerekkel, kivéve a 6. pontban felsoroltakat.
- Az oldat tiszta vagy kissé opálos lehet, sárgától a színtelenig, fény felé tartva buborékok lehetnek benne, de látható részecskét nem tartalmazhat. Az oldat megszűrése vagy felszívása után (lásd alább), az alkalmazás előtt az oldatot vizuálisan ellenőrizni kell. Zavaros, pelyhes csapadékot vagy részecskéket tartalmazó oldatot nem szabad felhasználni.
- Alkalmazás után a fel nem használt oldatot, a keletkezett hulladékot a helyi előírásoknak és az Ön kezelőorvosa által adott instrukcióknak megfelelően kell kezelni.
Feloldás
Az IDELVION port és az oldószert tartalmazó injekciós üvegeket bontatlanul melegítse szoba- vagy testhőmérsékletre. Ezt megteheti úgy, hogy az injekciós üvegeket egy órán keresztül szobahőmérsékleten tartja, vagy néhány percig a kezében tartva melegíti.
Az injekciós üvegeket direkt hő hatásának NE TEGYE KI. Az injekciós üvegeket tilos testhőmérsékletnél (37 °C) magasabb hőmérsékletűre melegíteni!
Óvatosan távolítsa el az injekciós üvegek védőkupakjait, és tisztítsa meg a szabaddá tett gumidugókat alkoholos törlőkendővel. Hagyja megszáradni az injekciós üvegeket mielőtt a Mix2Vial csomagot (elkészítéshez és beadáshoz szükséges készlet) kibontaná, majd az alábbiak szerint járjon el: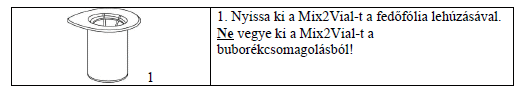
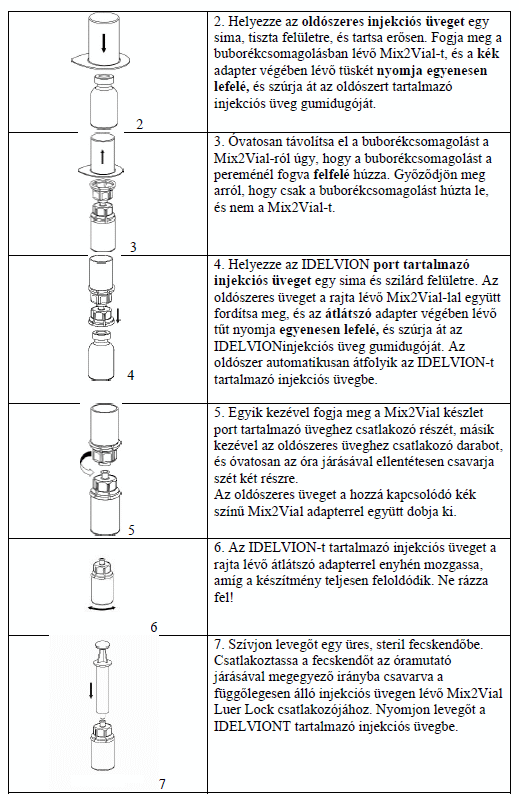
Felszívás és alkalmazás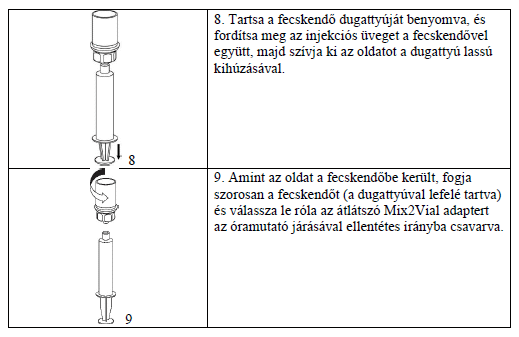
Használja a készítmény mellé adott vénapunkciós készletet, a készlet tűjét szúrja egy vénába. Engedje visszafolyni a vért a cső végéig. A fecskendőt csatlakoztassa a vénapunkciós készlet menetes zárású végéhez. Az elkészített oldatot lassan (ahogy Önnek kényelmes, de nem több mint 5 ml/perces sebességgel) fecskendezze a vénájába, a kezelőorvosától kapott utasításoknak megfelelően. Ügyeljen arra, hogy vér ne kerüljön a készítményt tartalmazó fecskendőbe.
Ellenőrizze önmagát, hogy jelentkeznek-e mellékhatásra utaló tünetek. Amennyiben az IDELVION beadásával kapcsolatba hozható mellékhatás lép fel, az injekció beadást le kell állítani (lásd még a 2. és 4. pontokat is).
A gyógyszer alkalmazásával kapcsolatos további kérdéseivel forduljon kezelőorvosához vagy gyógyszerészéhez.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Azonnal vegye fel a kapcsolatot a kezelőorvosával:
- ha Ön allergiás reakciók tüneteit észleli (lásd alább)
- ha Ön észleli, hogy a gyógyszer hatása nem megfelelő
A IX-es faktor tartalmú gyógyszerek alkalmazásánál az alábbi mellékhatásokat figyelték meg:
- allergiás típusú túlérzékenységi reakciók lehetségesek (gyakori) az alábbi tünetekkel: csalánkiütés, testszerte jelentkező bőrkiütés (generalizált urtikaria), mellkasi szorító érzés, sípoló légzés, alacsony vérnyomás (hipotónia) és anafilaxia (súlyos reakció, ami súlyos légzési nehézséget vagy szédülést okoz). Ha ez megtörténik, akkor hagyja abba a gyógyszer alkalmazását, és azonnal forduljon a kezelőorvosához.
- Inhibitorok: a gyógyszer nem hat megfelelően (folyamatos vérzés). Önnél is kialakulhat inhibitor (semlegesítő antitest) a IX-es faktor ellen (gyakoriság nem ismert), ebben az esetben a IX-es faktor hatása többé nem lesz megfelelő. Ha ez bekövetkezik, akkor hagyja abba a gyógyszer alkalmazását, és azonnal forduljon a kezelőorvosához.
Az alábbi mellékhatások gyakran előfordultak az IDELVION alkalmazásakor (10 betegből legfeljebb 1-et érinthetnek):
- fejfájás
- reakció az injekció beadás helyén
- szédülés
- kiütés
Az alábbi mellékhatások nem gyakran fordultak elő az IDELVION alkalmazásakor (100 betegből legfeljebb 1-et érinthetnek)
- ekcéma
Mellékhatások gyermekeknél és serdülőknél
Gyermekeknél a mellékhatások gyakorisága, típusa és súlyossága várhatóan ugyanolyan, mint felnőtteknél.
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti a https://mellekhatas.ogyei.gov.hu/ weboldalon. A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell az IDELVION-t tárolni?
- A gyógyszer gyermekektől elzárva tartandó!
- A címkén és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert.
- Legfeljebb 25 °C-on tárolandó.
- Nem fagyasztható!
- A fénytől való védelem érdekében az eredeti csomagolásban tárolandó.
- Az elkészített oldatot lehetőleg azonnal fel kell használni.
- Amennyiben az elkészített oldatot nem használják fel azonnal, a feloldás utáni (használat közbeni) tárolási időért és annak körülményeiért a felhasználó a felelős.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz az IDELVION?
A készítmény hatóanyaga:
Injekciós üvegenként 250 NE: 2,5 ml injekcióhoz való vízben történő feloldás után az oldat 100 NE/ml albutrepenonakog-alfa-t tartalmaz.
Injekciós üvegenként 500 NE: 2,5 ml injekcióhoz való vízben történő feloldás után az oldat 200 NE/ml albutrepenonakog-alfa-t tartalmaz.
Injekciós üvegenként 1000 NE: 2,5 ml injekcióhoz való vízben történő feloldás után az oldat 400 NE/ml albutrepenonakog-alfa-t tartalmaz.
Injekciós üvegenként 2000 NE: 5 ml injekcióhoz való vízben történő feloldás után az oldat 400 NE/ml albutrepenonakog-alfa-t tartalmaz.
Injekciós üvegenként 3500 NE: 5 ml injekcióhoz való vízben történő feloldás után az oldat 700 NE/ml albutrepenonakog-alfa-t tartalmaz.
Egyéb összetevők:
Nátrium-citrát, poliszorbát 80, mannit, szaharóz, sósav (pH beállításra).
Lásd az utolsó bekezdést a 2. fejezetben.
Oldószer: Injekcióhoz való víz
Milyen az IDELVION külleme és mit tartalmaz a csomagolás?
Az IDELVION halványsárga - fehér por és oldószerként injekcióhoz való vizet tartalmaz.
Az elkészített oldat tiszta vagy kissé opálos lehet, sárgától a színtelenig, fény felé tartva buborékok lehetnek benne, de látható részecskét nem tartalmazhat.
Kiszerelés
250, 500 vagy 1000 NE-t tartalmazó csomag:
1 port tartalmazó injekciós üveg
1 injekciós üveg 2,5 ml injekcióhoz való vízzel
1 db szűrővel ellátott áttöltő eszköz 20/20
Egy belső doboz tartalma:
1 db 5 ml-es egyszer használatos fecskendő
1 db vénapunkcióra szolgáló készlet
2 db alkoholos törlő
1 db nem steril tapasz
2000 vagy 3500 NE-t tartalmazó csomag:
1 port tartalmazó injekciós üveg
1 injekciós üveg 5 ml injekcióhoz való vízzel
1 db szűrővel ellátott áttöltő eszköz 20/20
Egy belső doboz tartalma:
1 db 10 ml-es egyszer használatos fecskendő
1 db vénapunkcióra szolgáló készlet
2 db alkoholos törlő
1 db nem steril tapasz
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A szöveg publikálásának dátuma az ema.europa.eu weboldalon: 2023.05.04.
 Nem áll rendelkezésre kép
Nem áll rendelkezésre kép Hatóanyag:
factor ix
Normatív TB-támogatás:
Eü. emelt támogatás:
Gyártó:
CSL Behring
Ár:
735919 Ft A feltüntetett ár tájékoztató jellegű
Kategóriák
ACNE-ELLENES KÉSZÍTMÉNYEK
ANTIBIOTICUMOK ÉS CHEMOTHERAPEUTICUMOK BŐRGYÓGYÁSZATI HASZNÁLATRA
ANTISEPTICUMOK ÉS FERTŐTLENÍTŐK
BŐRLÁGYÍTÓ- ÉS VÉDŐANYAGOK
CORTICOSTEROIDOK, BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
EGYÉB BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
GOMBÁSODÁS ELLENI BŐRGYÓGYÁSZATI SZEREK
GYÓGYSZERTARTALMÚ KÖTSZEREK
PSORIASIS ELLENI SZEREK
SEBEK ÉS FEKÉLYEK KEZELÉSÉRE SZOLGÁLÓ KÉSZÍTMÉNYEK
VISZKETÉS ELLENI SZEREK, BELEÉRTVE ANTIHISTAMINOK, ÉRZÉSTELENÍTŐK, STB.
ANTIDIABETIKUS TERÁPIA
ÁSVÁNYI ANYAGOK
DIGESTIVUMOK, BELEÉRTVE AZ ENZIMKÉSZÍTMÉNYEKET
ELHÍZÁS ELLENI SZEREK A DIÉTÁS KÉSZÍTMÉNYEK KIVÉTELÉVEL
EPE- ÉS MÁJBETEGSÉGEK GYÓGYSZEREI
ÉTVÁGYGERJESZTŐK
FOGÁSZATI KÉSZÍTMÉNYEK
FUNKCIONÁLIS GASTROINTESTINALIS BETEGSÉGEK ELLENI SZEREK
HÁNYÁSCSILLAPÍTÓK ÉS ÉMELYGÉS ELLENI SZEREK
HASMENÉSGÁTLÓK, VALAMINT A BÉL GYULLADÁSOS ÉS FERTŐZÉSES MEGBETEGEDÉSEINEK SZEREI
ROBORÁLÓ SZEREK
SAVTERMELÉS ZAVARÁVAL JÁRÓ BETEGSÉGEK GYÓGYSZEREI
SYSTEMÁS ANABOLICUMOK
SZÉKREKEDÉS ELLENI SZEREK
TÁPCSATORNA ÉS ANYAGCSERE EGYÉB GYÓGYSZEREI
VITAMINOK

Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja
Ⓒ Vidal Next kft. 2026.