HALIDOR 50 mg oldatos injekció
Betegtájékoztató
1. Milyen típusú gyógyszer a Halidor injekció, és milyen betegségek esetén alkalmazható?
A Halidor hatóanyaga, a benciklán, értágító és simaizom-görcsoldó vegyület. Érszűkülettel járó egyes betegségek, valamint a gyomor-bélrendszer, epehólyag, húgyhólyag, húgyvezeték görcsös állapotának kezelésére alkalmas.
2. Tudnivalók a Halidor injekció alkalmazása előtt
Ne alkalmazza a Halidor injekciót
Az alábbi kórállapotokban a Halidor alkalmazása ellenjavallt, ezért feltétlenül említse meg kezelőorvosának, ha a következők valamelyike vonatkozik Önre:
- ha allergiás a benciklánra, vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére,
- ha légzési elégtelensége van,
- ha súlyos vese- vagy májelégtelensége van,
- ha nem-egyensúlyban tartott (dekompenzált) szívelégtelensége van,
- ha heveny szívrohama van,
- ha szív-ingerületvezetési zavara van (AV-blokk),
- ha epilepsziás, vagy ha hajlamos epilepsziás jellegű görcsökre,
- ha agyvérzésen esett át a közelmúltban,
- ha koponya-/agysérülést szenvedett az elmúlt 12 hónapban.
Figyelmeztetések és óvintézkedések
A Halidor injekció alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A Halidor injekció ájuláshajlam esetén, valamint vizeletretencióval járó prosztata-megnagyobbodásban nem alkalmazható (a hólyagizomzat tónusának csökkentésével fokozza a retenció mértékét).
Tartós kezeléskor 2 havonta laborkontroll (májfunkció, fehérvérsejtszám-ellenőrzés) szükséges.
Egyéb gyógyszerek és a Halidor injekció
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett, valamint szedni tervezett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is.
A Halidor és egyes gyógyszerek kölcsönösen befolyásolhatják egymás hatását, ezért fokozott körültekintésre, esetleg az együtt szedett gyógyszerek adagjának módosítására lehet szükség.
Ezek a gyógyszerek a következők:
- altatók és nyugtatók - hatásuk fokozódik
- szívműködésre ható szerek:
- vízhajtók, kinidin, digitálisz, szimpatikomimetikumok (stresszhelyzetre hasonlító hatást kiváltó, idegrendszerre ható szerek) - szívritmuszavarok lehetősége fokozódik
- béta-blokkolók, mert együttadásakor a béta-blokkoló dózisát esetleg módosítani kell,
- kálciumcsatorna-blokkolók, vérnyomáscsökkentők - hatásuk fokozódik
- olyan gyógyszerek, amelyeknek mellékhatása az epilepsziás görcskészség fokozódása - a mellékhatás kockázatának fokozódása
- általános érzéstelenítők, valamint nyugtató/altató hatású gyógyszerek - hatásuk fokozódhat
- acetilszalicilsav - a véralvadásgátló hatás fokozódása.
A Halidor injekció nátriumot tartalmaz
A készítmény kevesebb, mint 1 mmol (23 mg) nátriumot tartalmaz ampullánként, azaz gyakorlatilag nátriummentes.
Terhesség és szoptatás
Állatkísérletek során magzatkárosító hatás nem igazolódott. Tekintettel arra, hogy megfelelő mennyiségű klinikai tapasztalat nem áll rendelkezésre, alkalmazása a terhesség első harmadában nem ajánlott. A terhesség további részében és a szoptatás alatt alkalmazása csak az előny/kockázat - orvos által történő - gondos egyedi mérlegelése után történhet.
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával vagy gyógyszerészével.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Alkalmazásának kezdeti szakaszában a gépjárművezetés, és a gépek kezelésével járó munkavégzés fokozott óvatosságot igényel. Ezt beszélje meg kezelőorvosával!
3. Hogyan kell alkalmazni a Halidor injekciót?
A készítmény ajánlott adagja:
A gyomor-bélrendszer, epehólyag, húgyhólyag, húgyvezeték heveny görcsös állapotaiban:
2-4 ampulla adása javasolt vénába (intravénás injekció), fiziológiás sóoldattal 10-20 ml-re hígítva és lassan befecskendezve, vagy 1 ampulla - hígítás nélkül - mélyen az izmokba (intramuszkularisan).
Érrendszeri megbetegedések:
A Halidor injekció infúzióban történő adagolása előnyös lehet, napi 200-300 mg-os adagban (4-6 ampulla), 2-3 részletben. Az infúziót lassan, kb. 1 óra alatt javasolt beadni.
Amennyiben többször kell alkalmazni a Halidor injekciót, az injekció beadásának helyét váltogatni kell.
Ha az előírtnál több Halidor injekciót kapott
A túladagolás tünetei:
Előfordulhat szapora szívverés, vérnyomásesés, ájulási hajlam, bevizelés, álmosság, nyugtalanság, súlyos esetben epilepsziaszerű görcsök.
Ha idő előtt abbahagyja a Halidor injekciós kezelést
Amennyiben a tervezettnél hamarabb hagyja abba a Halidor injekciós kezelést, a betegsége tünetei visszatérhetnek.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát vagy gyógyszerészét.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Immunrendszeri betegségek és tünetek: allergiás bőrtünetek (pl.: bőrkiütés).
Pszichiátriai kórképek: ritkán átmeneti zavartság, hallucinációk.
Idegrendszeri betegségek és tünetek: szórványosan nyugtalanság, fejfájás, szédülés, járászavar, kézremegés, álmosság, alvászavar, memóriazavar; nagyon ritkán központi idegrendszeri gócjelek (pl.: látászavar) jelentkezhetnek.
Szívbetegségek és a szívvel kapcsolatos tünetek: elvétve előfordulhat szívritmuszavar (főként más, erre hajlamosító gyógyszerrel való együttadáskor).
Emésztőrendszeri betegségek és tünetek: szájszárazság, gyomorfájdalom, teltségérzés, hányinger, hányás.
Általános tünetek, az alkalmazás helyén fellépő reakciók: rossz közérzet, testsúlynövekedés, intravénás alkalmazás esetén vénakárosodás (gyulladás, rögképződés).
Laboratóriumi vizsgálatok eredményei: eltérés a laboreredményekben (májenzimszint-emelkedés, fehérvérsejtszám-csökkenés).
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát vagy gyógyszerészét. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az V. függelékben található elérhetőségeken keresztül.
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Halidor injekciót tárolni?
A gyógyszer gyermekektől elzárva tartandó!
Legfeljebb 25 °C-on tárolandó.
A csomagoláson feltüntetett lejárati idő (Felh:) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
A készítmény gyártási számát, gyártási és lejárati idejét a dobozon találja.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Halidor injekció?
- A készítmény hatóanyaga: Minden ampulla 50 mg benciklán-hidrogénfumarátot tartalmaz.
- Egyéb összetevők: nátrium-klorid, injekcióhoz való víz.
Milyen a Halidor injekció külleme és mit tartalmaz a csomagolás?
2 ml-es, kristálytiszta, színtelen oldat, kék és sárga kódgyűrűvel ellátott átlátszó, törőponttal jelölt üvegampullában.
Csomagolás: 10 db ampulla/doboz.
Az ampulla kinyitása (jobbkezeseknél):
Tartsa az ampulla testét a bal kéz hüvelykujja és behajlított mutatóujja között. Az ampullára festett pont felfele nézzen (1. ábra)! Fogja az ampulla fejét a másik (jobb) kéz hüvelykujja és behajlított mutatóujja közé úgy, hogy a hüvelykujja takarja a pontot (2. ábra). Nyomja lefelé jobb keze hüvelykujját és bal kéz mutatóujjával tartson ellen, így gyakoroljon közepes és állandó erősségű hajlító mozdulatot anélkül, hogy a két kezét közelebb vinné egymáshoz, vagy távolítaná egymástól (3. ábra). Az ampulla nyaka a hajlítás kezdetétől bármikor eltörhet, anélkül, hogy a törést érezné (4. ábra).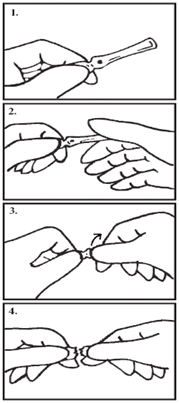
A betegtájékoztató engedélyezésének dátuma: 2016.04.01.
Hatóanyag:
bencyclane
Normatív TB-támogatás:
Eü. emelt támogatás:
Gyártó:
EGIS
Ár:
-
Kategóriák
ACNE-ELLENES KÉSZÍTMÉNYEK
ANTIBIOTICUMOK ÉS CHEMOTHERAPEUTICUMOK BŐRGYÓGYÁSZATI HASZNÁLATRA
ANTISEPTICUMOK ÉS FERTŐTLENÍTŐK
BŐRLÁGYÍTÓ- ÉS VÉDŐANYAGOK
CORTICOSTEROIDOK, BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
EGYÉB BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
GOMBÁSODÁS ELLENI BŐRGYÓGYÁSZATI SZEREK
GYÓGYSZERTARTALMÚ KÖTSZEREK
PSORIASIS ELLENI SZEREK
SEBEK ÉS FEKÉLYEK KEZELÉSÉRE SZOLGÁLÓ KÉSZÍTMÉNYEK
VISZKETÉS ELLENI SZEREK, BELEÉRTVE ANTIHISTAMINOK, ÉRZÉSTELENÍTŐK, STB.
ANTIDIABETIKUS TERÁPIA
ÁSVÁNYI ANYAGOK
DIGESTIVUMOK, BELEÉRTVE AZ ENZIMKÉSZÍTMÉNYEKET
ELHÍZÁS ELLENI SZEREK A DIÉTÁS KÉSZÍTMÉNYEK KIVÉTELÉVEL
EPE- ÉS MÁJBETEGSÉGEK GYÓGYSZEREI
ÉTVÁGYGERJESZTŐK
FOGÁSZATI KÉSZÍTMÉNYEK
FUNKCIONÁLIS GASTROINTESTINALIS BETEGSÉGEK ELLENI SZEREK
HÁNYÁSCSILLAPÍTÓK ÉS ÉMELYGÉS ELLENI SZEREK
HASMENÉSGÁTLÓK, VALAMINT A BÉL GYULLADÁSOS ÉS FERTŐZÉSES MEGBETEGEDÉSEINEK SZEREI
ROBORÁLÓ SZEREK
SAVTERMELÉS ZAVARÁVAL JÁRÓ BETEGSÉGEK GYÓGYSZEREI
SYSTEMÁS ANABOLICUMOK
SZÉKREKEDÉS ELLENI SZEREK
TÁPCSATORNA ÉS ANYAGCSERE EGYÉB GYÓGYSZEREI
VITAMINOK

Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja
Ⓒ Vidal Next kft. 2026.