SYNCUMAR MITE 1 mg tabletta
Betegtájékoztató
1. Milyen típusú gyógyszer a Syncumar és milyen betegségek esetén alkalmazható?
A Syncumar tabletta a kumarin típusú véralvadásgátló gyógyszerek közé tartozik, melyek akadályozzák a K-vitamin felhasználását. Hatása következtében nem képződik kellő mennyiségű hatékony, a véralvadás során felhasználható faktor, így a véralvadás lassabb lesz. A jól beállított Syncumar-kezelés időtartama alatt állandó és egyenletes véralvadásgátlás alakul ki, mely csökkenti a vérrögképződés és a nagyobb vérzések bekövetkezésének valószínűségét.
A Syncumar felnőttek esetében alkalmazható:
- különféle betegségek következtében a visszerekben (vénákban) kialakuló véralvadékok képződésének (mélyvénás trombózis), illetve az ezekből leszakadó és a tüdő ereiben megakadó rögök (tüdőembólia) kialakulásának megelőzésére és következményeinek kezelésére;
- a szívben, illetve a verőerekben kialakuló véralvadékok képződésének és az ezekből leszakadó és a különböző szervekben (agy, végtagok, hasi erek, vese) megakadó rögök, úgynevezett embóliák okozta érelzáródás kialakulásának megelőzésére olyan felnőtteknél, akiknél az alábbi betegségek bármelyike előfordul:
-- pitvarfibrilláció,
-- a bal szívfélben a pitvar-kamrai határon lévő kéthegyű billentyű szűkülete a vér kóros visszaáramlásával vagy anélkül (mitrális sztenózis és/vagy mitrális regurgitáció),
-- a szívüregek kitágulásával járó szívizombántalom (dilatatív kardiomiopátia),
-- biológiai és mechanikus műbillentyű beültetése utáni állapot,
-- a kórelőzményben szereplő szívinfarktus.
- szívinfarktus másodlagos megelőzése.
A Syncumar adagja betegenként változhat, és a kezelés során ugyanannál a betegnél sem mindig állandó. A Syncumar véralvadásgátló hatását a protrombinidő (PI), illetve a nemzetközi normalizált arány (angol rövidítése: INR) mérésével határozzák meg. Minél nagyobb az INR értéke, annál lassabb a véralvadás. A gyógyszer szedésének kezdetén, vagyis a terápiás adag beállításakor, gyakrabban (akár hetente többször is), később ritkábban (kéthetente, havonta) kell meghatározni az INR-t. A véralvadásgátlás mértékét kifejező INR-érték általában 2-3 között mozog. Kezelőorvosa indokolt esetben ennél nagyobb értéket is szükségesnek tarthat.
A betegtájékoztató 2. és 3. pontjában az egyes szakaszok mellett az 1. táblázatban szereplő jelzéseket találja, melyek a gyógyszer helyes alkalmazására és a véralvadásgátlás kialakulásával kapcsolatos veszélyekre hívják fel a figyelmét.
2. Tudnivalók a Syncumar alkalmazása előtt
Ne szedje a Syncumar-t, amennyiben
- allergiás (túlérzékeny) a gyógyszer hatóanyagára, egyéb kumarinszármazékokra, vagy a gyógyszer bármely segédanyagára,
- Ön várandós,
- testének bármely részéből vérzik, például sebekből, testbe helyezett eszközökből, sérülésekből,
- kiterjedt, súlyos sérülései vannak,
- bármilyen más okból Önnél már véralvadásgátló kezelést kezdtek el, és azt jelenleg is folytatják,
- a közelmúltban a fejében (a koponyaűrben) vérzés következett be, vagy olyan elváltozások állnak fenn, melyek az ilyen típusú vérzés kialakulásának kockázatát fokozzák (például agyi értágulat, úgynevezett intrakraniális aneurizma),
- gerinc körüli érzéstelenítést végeztek a gyógyszer megkezdését megelőző 1 napon belül, vagy úgynevezett epidurális katétere van (például fájdalomcsillapítás céljából),
- ha nem lehet elvégezni a kezelés ellenőrzéséhez szükséges INR-vizsgálatokat (általában együttműködésre valamely okból képtelen betegek esetében),
- a következők valamelyike érvényes az Ön esetében, és kezelőorvosának véleménye szerint nem kaphat Syncumar-kezelést, mivel a kezelés következtében kialakuló vérzés veszélye meghaladja a kezelésből származó lehetséges előnyöket:
-- a kezelőorvos értékelése szerint jelentős a vérlemezkék számának csökkenése, vagy azok működési zavara áll fenn - mely fokozza a vérzés veszélyét;
-- kórelőzménye arra utal, hogy - bármely betegség miatt - gyakran elesik, vagy ennek valószínűsége nagy - mivel vérzésforrásként szereplő külső vagy belső sérülések alakulhatnak ki;
-- lehetséges vagy igazolt vérzési hajlama van - mely fokozza a vérzés veszélyét;
-- hashártyája vagy mellhártyája rosszindulatú daganat terjedése miatt gyulladásban van;
-- a vékonybélbe vezetett szondán át táplálják;
-- belei bármely szakaszán kesztyűujjszerű kitüremkedések vannak (úgynevezett divertikulitisz);
-- bőrén át bárhol szövetminta nyerése céljából tűvel megszúrták (például a gerinccsatornából folyadék vagy a májból szövetminta vételére, úgynevezett lumbálpukció, illetve májbiopszia);
-- lehetséges vagy igazolt vérképzőszervi betegsége van - mely fokozza a vérzés veszélyét;
-- a közelmúltban központi idegrendszeri sebészeti beavatkozást (például agyműtét vagy gerincműtét) vagy szemműtétet végeztek Önnél;
-- kiterjedt szöveti érintettséggel járó, szövetkárosító hatású sebészeti beavatkozást (égéssebészeti beavatkozások és más altatásban végzett műtétek) végeztek, vagy tudja, hogy végezni fognak a kezelése során - mely fokozza a vérzés veszélyét;
-- a húgyutakból, légutakból, illetve a tápcsatornából vérzik, vagy ezekben fekélyképződés áll fenn, vagy akárcsak a lehetősége is fennáll, hogy ez bekövetkezik - mert a véralvadásgátlás hatására megindulhat vagy fokozódhat a vérzés;
-- nem vagy eredménytelenül kezelt magasvérnyomás-betegségben (úgynevezett malignus hipertónia) szenved, és vérnyomása tartósan magas - mely fokozza az agyvérzés veszélyét;
-- súlyos májkárosodásban vagy vesekárosodásban szenved - mely fokozza a vérzés veszélyét;
-- akut szívburokgyulladása van - mely fokozza a vérzés veszélyét;
-- a szívburokban folyadék van - mely fokozza a vérzés veszélyét;
-- a szív vagy a vérerek kisebb-nagyobb területen jelentősen kitágultak - úgynevezett aneurizma, mely kiszakadhat;
-- fertőzéses szívbelhártya-gyulladása van - mely fokozza a vérzés veszélyét;
-- tüdő-, prosztata- vagy méhműtétet követően fokozódott a véralvadék feloldódása (úgynevezett fokozott fibrinolízis áll fenn) - mely fokozza a vérzés veszélyét;
-- már alkalmaztak Önnél más, a Syncumar-hoz hasonló gyógyszert (úgynevezett K-vitamin-antagonistát, például warfarint), és a kezelés során bőrelhalás vagy lágyszövetelhalás alakult ki.
Figyelmeztetések és óvintézkedések
A Syncumar alkalmazása előtt beszéljen kezelőorvosával, gyógyszerészével, vagy a gondozását végző egészségügyi szakemberrel.
Fogamzóképes nőknél a kezelés megkezdése előtt terhességi tesztet kell végezni az esetleges terhesség tisztázása végett.
Valamely véralvadásgátlóról egy másikra való áttérés nagymértékben megnöveli a vérzés kockázatát az áttérés időszakában, amikor a két gyógyszert egyszerre adják.
A kezelés megkezdése előtt a gyógyszert rendelő orvost tájékoztatni kell minden korábbi, illetve jelenleg fennálló betegségről, valamint a máj- és vesefunkció, a kezelés előtti protrombinidő és a vércsoport meghatározása szükséges.
Gyermekek és serdülők
A Syncumar csak felnőttek kezelésére alkalmazható.
Egyéb gyógyszerek és a Syncumar
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket és étrendkiegészítőket is.
A Syncumar-ral folytatott kezelés idején kizárólag olyan gyógyszereket szabad szednie, melyek alkalmazásával kezelőorvosa egyetértett, illetve melyeket előírtak az Ön számára. A Syncumar-ral kezelt betegek esetében más gyógyszer bevezetésekor vagy annak abbahagyásakor a betegeket nagyon körültekintően kell ellenőrizni.
A Syncumar tabletta egyidejű alkalmazása étellel, itallal és alkohollal
Szeszesitalok fogyasztása:
A Syncumar szedésének idején legfeljebb napi 150 ml könnyű bor, vagy más - hasonló alkoholtartalmú, napi adagban legfeljebb kb. 15 g etilalkoholt tartalmazó - nem tömény ital fogyasztható.
K1-vitamin-szükséglet:
Étrendje mindennap tartalmazzon férfiaknál 120 mikrogramm, nőknél 90 mikrogramm K1-vitamint. Ennyi K-vitamin fogyasztása elegendő. Ezt a mennyiséget mind a négy évszakban naponta el kell fogyasztani. Fontos, hogy a Syncumar-kezelés során az étrend K-vitamin tartalma legyen egyenletes.
K-vitamin-tartalmú élelmiszerek, étrendkiegészítők, tápszerek
Nagy mennyiségű K1-vitamint tartalmaznak a friss és szárított zöldleveles növények. Általánosságban mondható, hogy minél zöldebb a levél, melyből az étel készül, annál magasabb a K1-vitamin-tartalma (például kel, zsázsa, spenót, bazsalikom, endívia, metélőhagyma, újhagyma, kelbimbó, fejes saláta, brokkoli, kelkáposzta).
Kérjük, olvassa el az élelmiszerek, étrendkiegészítők, tápszerek címkéjén található információt, hogy tartalmaznak-e K-vitamint. A csontritkulás megelőzésére javasolt étrendkiegészítők és az úgynevezett multivitamin-készítmények tartalmaznak gyakran K-vitaminokat.
Csak akkor fogyasszon ilyen összetevőket tartalmazó élelmiszereket, étrendkiegészítőket, tápszereket, ha egészsége védelmében feltétlenül szüksége van rá, és ha kezelőorvosa is egyetért ezzel.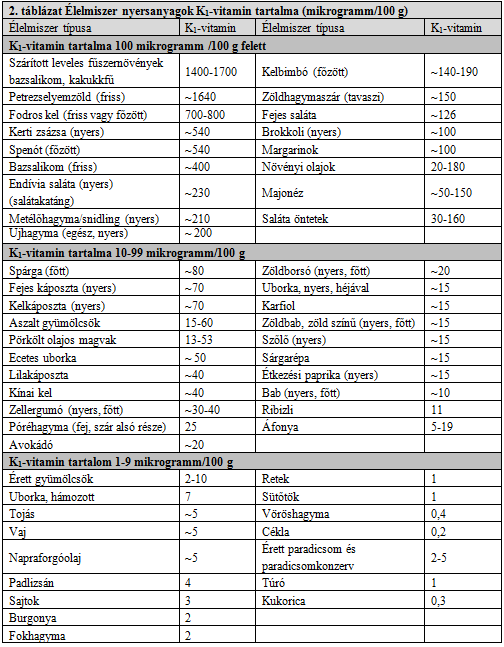
Terhesség, szoptatás és termékenység
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával.
A készítmény szedése terhesség alatt ellenjavallt (magzatkárosító hatás előfordulása, vérzésveszély miatt)!
Fogamzóképes nőknek biztonságos - lehetőleg kettős, például óvszer és pesszárium, vagy méhen belüli eszköz - fogamzásgátló módszer alkalmazása szükséges a Syncumar tabletta szedése folyamán.
Amennyiben Syncumar-kezelés alatt áll és gyermeket szeretne, kezelőorvosa segítségével gondosan válassza meg a fogantatás időpontját. A fogantatás előtt a Syncumar-kezelést abba kell hagyni, és a gyógyszer kiürüléséhez kellően hosszú időszaknak kell eltelnie.
Fennálló terhességét vagy akár a terhesség gyanúját azonnal tudassa kezelőorvosával.
A szoptatás ideje alatt, kivételes esetben, orvosi javaslatra és az anya és a gyermek rendszeres, gyakori orvosi ellenőrzése mellett alkalmazható. Az esetleges - a gyermeknél kialakuló - véralvadásgátló hatás megelőzése végett a gyermeknek megelőző K1-vitamin-kezelést kell adni.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
Nincs adat arra vonatkozóan, hogy a Syncumar tabletta hatással lenne a gépjárművezetésre vagy a baleseti veszéllyel járó munka végzésére.
A Syncumar laktózt tartalmaz
Ez a gyógyszer tejcukrot (laktóz) tartalmaz. Egy Syncumar mite 1 mg tabletta 48,3 mg laktózt tartalmaz. Amennyiben kezelőorvosa korábban már figyelmeztette Önt, hogy bizonyos cukrokra érzékeny, keresse fel orvosát, mielőtt elkezdi szedni ezt a gyógyszert.
3. Hogyan kell a Syncumart alkalmazni?
A Syncumar tablettát mindig a kezelőorvosa által elmondottaknak megfelelően szedje. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Az orvos által előírt napi adagot egyszerre, azonos időben, szájon át kell bevenni.
A gyógyszer szokásos adagja a kezelés megkezdésekor 4 mg körül van (4 darab Syncumar mite 1 mg tabletta), melyet néhány napig injekcióban adott véralvadás-csökkentővel kombinálnak. Ezután a Syncumar-adagot a felére (2 mg) csökkenthetik. Általában ennyi a fenntartó adag is. A jól beállított kezelés jellemzője az, hogy a 3. hónaptól havonta vagy gyakrabban végzett INR-meghatározások eredménye egy fél év adatait összegezve (például a 4-9. hónap időszakában, legalább 7 mérés eredményét tekintve) 2,0-3,0 között van a mérések legalább 60%-ában (legalább 5 esetben). Amennyiben egy féléves időszakban a mérések kevesebb mint 60%-ában van az INR értéke a megállapított tartományban, akkor enyhén módosítani kell a beállítást.
Ne hagyja abba a gyógyszer szedését kezelőorvosa jóváhagyása nélkül. Önkényesen ne változtassa meg a Syncumar tabletta adagját, mert veszélyes szövődmények léphetnek fel (trombózis, embólia vagy vérzés)!
A kezelés időtartama:
A véralvadásgátló kezelés az alapbetegség típusától függően 3-6 hónaptól akár évekig is tarthat, fenntartása akár a teljes élettartam alatt szükséges lehet.


Betegségek:
A kezelés folyamán a kezelőorvost tájékoztatni kell a közbejött betegségekről (még a legenyhébbnek tűnőkről is, mint hasmenés, láz).
A kezelés során alkalmazott egyéb gyógyszerek (lásd még 2. pont):
A kezelés folyamán a kezelőorvost tájékoztatni kell, ha bármilyen - akár vény nélkül kapható - új gyógyszert kezd szedni, vagy a régiek közül valamelyiket abbahagyja, mert szükségessé válhat a Syncumar-adag módosítása. Amennyiben szükséges, kezelőorvosa ilyenkor INR-ellenőrzést ír elő, és ennek alapján megváltoztathatja a korábban javasolt gyógyszeradagot. A gyakran alkalmazott gyógyszerek (például láz- és fájdalomcsillapítók) alkalmazásáról egyeztessen előre kezelőorvosával. Így biztosabban tud dönteni, ha sürgős esetben gyógyszert kell bevenni.
Alkalmazás gyermekeknél és serdülőknél
A Syncumar gyermekek és serdülők kezelésére nem alkalmazható.
Ha idő előtt abbahagyja a Syncumar alkalmazását
A Syncumar alkalmazását csak kezelőorvosának egyetértésével hagyja abba. Növeli a vérrögképződés és a vérrög leszakadásának kockázatát, ha a tervezett kezelési időt nem tartja be.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így a Syncumar is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Gyakori mellékhatások (10 betegből legfeljebb 1 beteget érinthet):
Vérzés (orrvérzés vagy fogínyvérzés, vagy véraláfutás); valamint véres vizelet, fekete vagy véres széklet, fokozott vagy elnyújtott menstruációs vérzés. Kórházi ellátást igénylő jelentős vérzések is lehetnek. Vérszegénység.
Ritka mellékhatások (1000 betegből legfeljebb 1 beteget érinthet):
Allergiás reakciók (csalánkiütés, bőrkiütés) érgyulladás, koleszterinembolizáció a lábujjak lila elszíneződésével ("lila ujj" szindróma), étvágytalanság, hányinger, hányás, hasmenés, hasnyálmirigy-gyulladás, a májenzimek szintjének átmeneti emelkedése, hajhullás, vérzéses bőrelhalás (lilásvörös és fájdalmas bőrelváltozások a talpon és lábujjakon). Láz.
Nem ismert gyakoriságú mellékhatások (a gyakoriság a rendelkezésre álló adatokból nem állapítható meg):
Fehérvérsejtek hiánya, úgynevezett eozinofil sejtek felszaporodása, fejfájás, érfali meszesedés, fájdalmas bőrkiütés. A Syncumar ritka esetekben súlyos bőrproblémákat okozhat, ideértve a kalcifilaxist is, amely fájdalmas bőrkiütéssel kezdődhet, de súlyos szövődményekhez vezethet. Ez a mellékhatás gyakrabban jelentkezik súlyos vesebetegségben szenvedő betegeknél. Vérzés a vesében, néha vér jelenlétével a vizeletben, ami a vese nem megfelelő működéséhez vezet (antikoagulánsokkal összefüggő nefropátia).
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az alábbi elérhetőségek valamelyikén keresztül:
Nemzeti Népegészségügyi és Gyógyszerészeti Központ, Postafiók 450, H-1372 Budapest
honlap: https://ogyei.gov.hu
elektronikus bejelentő form: https://mellekhatas.ogyei.gov.hu/
e-mail: adr.box@nngyk.gov.hu
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Syncumar-t tárolni?
Syncumar mite 1 mg tabletta:
Legfeljebb 30 °C-on tárolandó. A nedvességtől való védelem érdekében az eredeti csomagolásban tárolandó.
A gyógyszer gyermekektől elzárva tartandó!
A címkén feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Syncumar tabletta?
- A készítmény hatóanyaga:
Syncumar mite 1 mg tabletta: 1 mg acenokumarolt tartalmaz tablettánként.
- Egyéb összetevők:
Syncumar mite 1 mg tabletta: magnézium-sztearát, zselatin, talkum, burgonya-keményítő, laktóz-monohidrát (48,3 mg).
Milyen a Syncumar tabletta külleme és mit tartalmaz a csomagolás?
Küllem:
Syncumar mite 1 mg tabletta: fehér, kerek, mindkét oldalán lapos, metszett élű, egyik oldalán mélynyomású "SYNCU" jelöléssel, másik oldalán törővonallal ellátott tabletta. A tabletta egyenlő adagokra osztható.
Csomagolás:
Syncumar mite 1 mg tabletta:
3×10 db, illetve 6×10 db, illetve 9×10 db tabletta PVC//Al buborékcsomagolásban és dobozban.
A betegtájékoztató engedélyezésének dátuma: 2025.06.01.

Hatóanyag:
acenocoumarol
Normatív TB-támogatás:
Eü. emelt támogatás:
Gyártó:
Bausch Health Ireland
Ár:
765 Ft A feltüntetett ár tájékoztató jellegű
Hatóanyag:
acenocoumarol
Normatív TB-támogatás:
Eü. emelt támogatás:
Gyártó:
Bausch Health Ireland
Ár:
-
 Nem áll rendelkezésre kép
Nem áll rendelkezésre kép Hatóanyag:
acenocoumarol
Normatív TB-támogatás:
Eü. emelt támogatás:
Gyártó:
Bausch Health Ireland
Ár:
2195 Ft A feltüntetett ár tájékoztató jellegű
Kategóriák
ACNE-ELLENES KÉSZÍTMÉNYEK
ANTIBIOTICUMOK ÉS CHEMOTHERAPEUTICUMOK BŐRGYÓGYÁSZATI HASZNÁLATRA
ANTISEPTICUMOK ÉS FERTŐTLENÍTŐK
BŐRLÁGYÍTÓ- ÉS VÉDŐANYAGOK
CORTICOSTEROIDOK, BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
EGYÉB BŐRGYÓGYÁSZATI KÉSZÍTMÉNYEK
GOMBÁSODÁS ELLENI BŐRGYÓGYÁSZATI SZEREK
GYÓGYSZERTARTALMÚ KÖTSZEREK
PSORIASIS ELLENI SZEREK
SEBEK ÉS FEKÉLYEK KEZELÉSÉRE SZOLGÁLÓ KÉSZÍTMÉNYEK
VISZKETÉS ELLENI SZEREK, BELEÉRTVE ANTIHISTAMINOK, ÉRZÉSTELENÍTŐK, STB.
ANTIDIABETIKUS TERÁPIA
ÁSVÁNYI ANYAGOK
DIGESTIVUMOK, BELEÉRTVE AZ ENZIMKÉSZÍTMÉNYEKET
ELHÍZÁS ELLENI SZEREK A DIÉTÁS KÉSZÍTMÉNYEK KIVÉTELÉVEL
EPE- ÉS MÁJBETEGSÉGEK GYÓGYSZEREI
ÉTVÁGYGERJESZTŐK
FOGÁSZATI KÉSZÍTMÉNYEK
FUNKCIONÁLIS GASTROINTESTINALIS BETEGSÉGEK ELLENI SZEREK
HÁNYÁSCSILLAPÍTÓK ÉS ÉMELYGÉS ELLENI SZEREK
HASMENÉSGÁTLÓK, VALAMINT A BÉL GYULLADÁSOS ÉS FERTŐZÉSES MEGBETEGEDÉSEINEK SZEREI
ROBORÁLÓ SZEREK
SAVTERMELÉS ZAVARÁVAL JÁRÓ BETEGSÉGEK GYÓGYSZEREI
SYSTEMÁS ANABOLICUMOK
SZÉKREKEDÉS ELLENI SZEREK
TÁPCSATORNA ÉS ANYAGCSERE EGYÉB GYÓGYSZEREI
VITAMINOK

Az adatokat a PHARMINDEX gyógyszer-információs adatbázis szolgáltatja
Ⓒ Vidal Next kft. 2026.